 |
||||
| Навигация | |||||||||||||||
| Администрация | Студентам | Абитуриентам | Форум | Новости | Карта сайта | Создатели | |||||||||
|
11.4 Атом водорода согласно квантовой механики. Квантовые числа электрона в атоме Результаты полученные согласно теории Бора в решении задачи об энергетических уровнях электрона в водородоподобных атомах, получены в квантовой механике без привлечения постулатов Бора. Покажем это. Состояние электрона в водородоподобном атоме описывается некоторой волновой функцией y, удовлетворяющей стационарному уравнению Шредингера [см.(9.22)]. Учитывая, что потенциальная энергия электрона где r - расстояние между электроном и ядром, получим уравнение Шредингера в виде
Целесообразно воспользоваться сферической системой координат r, q, j и искать решение этого уравнения в виде следующих собственных функций
где n, l, m - целочисленные параметры собственных функций. При этом n - называют главным квантовым числом, l - орбитальным (азимутальным) и m - магнитным квантовым числом. Доказывается, что уравнение (12) имеет решение только при дискретных отрицательных значениях энергии где n = 1, 2, 3,... главные квантовые числа. |
||||
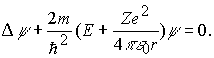 (12)
(12)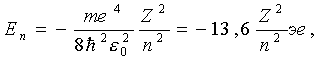 (14)
(14)