|
||||
| Навигация | |||||||||||||||
| Администрация | Студентам | Абитуриентам | Форум | Новости | Карта сайта | Создатели | |||||||||
|
11.3. Линейчатый спектр атома водорода Спектр излучения атомарного водорода состоит из отдельных спектральных линий, которые располагаются в определенном порядке. В 1885 г. Бальмер установил, что длины волн (или частоты) этих линий могут быть представлены формулой. Действительно, из (7) с учетом (6) для водорода (Z = 1), следует, что
где R = 2,07× 1016 с -1 - постоянная Ридберга Учитывая, что 1/l = v/с = w/2pс и используя (8), найдем
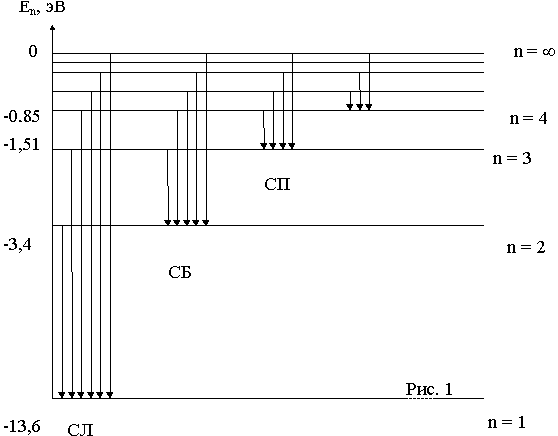
где R =1,0974×107 м-1 - называется также постоянной Ридберга. На рис. 1 изображена схема энергeтических уровней атома водорода, расчитанных согласно (6) при z=1.
При переходе электрона с более высоких энергетических уровней на уровень n = 1 возникает ультрофиолетовое излучение или излучение серии Лаймана (СЛ). Когда электроны переходя на уровень n = 2 возникает видимое излучение или излучение серии Бальмера (СБ). При переходе электронов с более высоких уровней на уровень n = 3 возникает инфракрасное излучение, или излучение серии Пашена (СП) и т.д. Частоты или длины волн, возникающего при этом излучения, определяются по формулам (8) или (9) при m=1 - для серии Лаймана, при m=2 - для серии Бальмера и при m = 3 - для серии Пашена. Энергия фотонов определяется по формуле (7), которую с учетом (6) можно привести для водородоподобных атомов к виду : Теория Бора сыграла огромную роль в создании атомной физики.В период ее развития (1913 - 1925 г.) были сделаны важные открытия , например, в области атомной спектроскопии. Однако в теории Бора обнаружились существенные недостатки, например, с ее помощью невозможно создать теорию более сложных, чем атом водорода, атомов. Поэтому становилось очевидным, что теория Бора представляет собой переходной этап на пути создания последовательной теории атомных и ядерных явлений. Такой последовательной теорией явилась квантовая (волновая) механика. |
||||
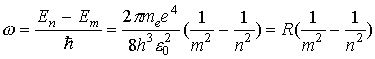 , (8)
, (8)